Процентът мол - Референтен химик 21
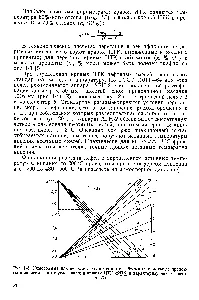
Фиг. 1-3. А номограма за превръщане на насипни дестилат фракция в молни процента в зависимост от ъгъла на наклона на кривата и MK CTI и характеризиране фактор (К).
Моларната част се нарича също моларно или молекулна, глупав или фракция. Е равна на 100 молни процента Ni. [C.296]
Концентрацията, изразена в мол процента (й%), е съотношението на броя на моловете на компонент rij / TII мола на сумата на всички компоненти на сместа, умножено по 100 [c.103]
Преизчисление концентрация разтворено вещество. изразена в грам-еквивалента на 1 литър разтвор (SD) в молни проценти - концентрация, изразена в грам-молекули на веществото на 100 г-мол разтвор (W), може да се направи с формулата [C.13]
ПРИМЕР Пример Изчисли равновесната степен на превръщане на азот и водород на амоняк при температура от 427 ° С и налягане от 300 атм. първоначалния състав на газа в молни процента азот 25%, водород 757o. Реакцията протича съгласно уравнението [С.18]
Както се вижда от таблицата, разтворимостта на така наречените постоянни газове (HJ, N2, CO, O 2) е малък (няколко стотни и няколко десети от процента от мол). Относително високата разтворимост на етилен, въглероден диоксид, хлор дължи на факта, че критичните температури на тези газове са високи и близки до критичната температура на разтворителя. от една и съща стойност за постоянните газове. [C.225]
По-удобно да се идентифицират модели в свойствата на решения не е сравнение тегло количества от компонентите. и техните моларни количества. при което в този случай съставът може да бъде изразена в мол фракции. и мол процента. [C.295]
Молни процента - брой молове от вещество, разтворено в 100 гр-мол разтвор. [В.12]
K - моларна процент от неизгоряло гориво в продуктите на горенето. [С.10]
CO2, O2 - моларен процент на отделните вещества в горива [c.54]
Използването на Номограмата се илюстрира с примера на фиг. 22 е необходимо да се определи колко молни процента съответства на 30% (тегл.) Бензен в бензен-толуен смес. Известно е, че за бензол = 78.11, и толуен за М = 92.13. След 78,11 / 92,13 = 0,848 0,85. [C.37]
Н мол процент на неизгоряло гориво в димните газове. [C.54]
Състав на сместа винаги изразяват концентрация летлив компонент. ако не е посочено конкретно. Концентрация посочено в обем, тегло или мол фракции или в по-голямата част, масата или мол процента. [C.34]
Ако ние считаме, хоризонталните редове I и II на RNS. 43, за които по абсцисата диаграмите посочени концентрация в молни процента на базата на високо летлив компонент (вж. Също фиг. 29), могат да бъдат идентифицирани следните отношения. [C.72]
В триъгълна схема. Съставите на смесите изобразени с използване Гибс триъгълник върховете характеризират неговите чисти компоненти А, В и 5, и се нанасят върху страните на теглото (понякога мола) проценти. Фиг. XI1-1 триъгълни диаграми представени най-често срещаните видове трикомпонентни смеси първия [c.388]
Какво представлява молни процента алкен-ароматен въглеводород-позиция на изопропилбензол в следните реакции при 1000 ° К и 1 атмосфера, ако един мол от кумол се приема за реакцията [c.215]
Ако циклопентан и неговите производни не са предварително merizovat в изо-St-пръстенна структура, след това дехидриране те не образуват ароматен въглеводород [256, 257]. Докато термодинамичните условия при температура над 300 ° С са благоприятни за образуването на ароматни въглеводороди [258], по време на топлинна обработка циклохексанови ароматни съединения не се образуват. При температура 550 ° С, произведен много малки количества бензол, [259], и при 620 ° С добивът на ароматни съединения е само 0.4 молни процента, въпреки факта, че разграждането претърпява крекинг до 24% циклохексан [260]. Частично алкилови производни на циклохексил [c.101]
Кондензацията на ацетон може да се получи изофорон. използван като разтворител. Що се отнася до мол процента от теоретичния добив ще варира. ако не се вземе предвид, че състоянието на несъвършена система. Реакцията се провежда RCT 500 ° К и 35 атм с 3 мола ацетон [c.219]
В по-горе (стр. 485 и сл.) Изчисляване на броя на теоретичните етапи чрез у-схема позволява равни моларни топлини на изпаряване на компонентите и последващо количеството на постоянството на течност и пари в височина дестилационна колона. В се наблюдава За това предположение, материалът трябва да се извършва изчисления, експресиращи всички стойности или Kmol молни процента, поради необходимостта да се преизчисли в тегловни единици за мол. В допълнение, когато се изчислява съгласно схема X-Y не се включват топлина. снабден с или загуби чрез дестилация. [C.502]
Налягане, кг / CL 2 молни процента на метан в smesn [c.97]
Задоволителни резултати могат да бъдат получени за системи, съдържащи малки количества от азот и въглероден диоксид [4, 5, 6, 28, 29], когато се прилага за действителното молекулно тегло от азот и въглероден диоксид. Фиг. 22 илюстрира споразумение между получените и изчислените стойности на константите на равновесие за метана в трите трикомпонентни системи. съдържащ 5 молни процента азот при 26,7 ° С точките показват експерименталните данни за кривите на равновесие - стойности. изчислена от графиките, основа за изграждането на които е поставен парафин система. Максималното отклонение между изчислените и наблюдавани равновесни константи за метана в този случай [4, 5, 6] равно на 5%. [C.111]
Моларната част може да бъде изразена в части от единица, и като процент (в последния случай, тя се нарича мол процента). [C.179]
Kontsengratsiya в мол фракции определя само от състава и фаза не е зависима от температурата и налягането. Ако стойността се умножава по 100, за да се получи концентрация на компонента в молни процента (мол ° / о). [C.207]
температура на кристализация в сравнение. Състав на сместа се изразява графично. За тази цел, оста на абсцисата представлява състав в тегловни или молни процента, и температурата на топене на у-ос (кристализация). Тази графика се нарича диаграма fusibility. [C.41]
Бутан. п-Butanizomerizuetsyav YuOraz бързо от izobutap [422]. В течната фаза с добавяне на 5 молни процента на катализатор (алуминиев бромид) при 27 ° С под налягане от 3 kPsm равновесна смес от п-бутан и изобутан съдържа около 78- 82% от него. Задължително 1000 часа за достигане на това състояние, няма други продукти се образуват и катализатора остава непроменена [411, 423, 424]. Скоростта на реакцията зависи от температурата и катализатор концентрация. При високи температури са забележима реакция преразпределение. [C.117]
Преразпределението реакционни свързани двойни връзки във всички случаи са лесно получени по-високи или по-ниски алкил-заместени продукти. Например, ксилени претърпяват преразпределение в присъствието на флуороводород. борен трифлуорид или алуминиев хлорид [501], за да се образува бензен, толуен и високи алкилирани продукти. Правилният избор на условията за преразпределение може да се извърши количествено. По този начин, в присъствието на 90 молни процента борен трифлуорид етилбензен образува смес от бензол и [c.126]
От диаграма на úrad от Hv (фиг. 61) може лесно да се види, че в концентрацията на ниско компонент на кипене по-малко от 10% (мол.) Намаляване на концентрацията на мол процент изисква значително увеличение на броя oroshayush, че течност. На практика, дестилация обикновено започва в съотношение кипене на п = 2, и температурата се повишава до върха на колоната [c.102]
Изомеризация окислители. През 1963-65. от Henkel (Германия), разработен метод за получаване на терефталова киселина с висока чистота калиеви соли на фталова или изофталова киселина. Схемата на процеса, показан на фиг. 3.16. Сухи в апарата I калиева сол. не съдържа кристализационна вода. Той се пропуска през реактора 2 в ОВ атмосфера при 400-430 ° С под налягане от 0.5-2.0 МРа в присъствието на кадмий катализатор частици. взето в количество от няколко процента от мол. При тези условия на степента на конверсия на суровината е почти 100% добив dikaliytereftalata достига 95-98%. [C.94]
Пример. Разтворът съдържа 1000 грама вода 100 г KNO3, 200 грама и 150гр Nanog КС1. Определяне на състава на разтвор) соли на грам молекули на 1000 г-мол вода, б) в молни процента, в) в еквивалент процент и г) в йонен еквивалент процент. [С.18]
В уравнение (VI-16) не е включен peidealnost пара и течни фази, така че налягането трябва да бъде ниска, и разтворимостта на малки, в повечето случаи по-малко от един мол процента. За разлика от коефициентите Бунзенова при изчисляването на Ostwald коефициенти и обема на газ се смесва при температура на система. По този начин и чрез заместване на уравнение (VI-16) следва да се отбележи, че [c.81]
Налягане, кг / SL12 на мол процента на метан в смес [c.97]
U 20 30 40 50 60 70 80 90 100 молни процента на азот в течна dzaze [c.98]